近期,国内外疫情均出现反复,世界衞生组织总干事谭德塞7月12日在日内瓦表示,由于变异新冠病毒的流行和疫苗供应的不均衡,全球新冠疫情再度面临严峻态势。
在未来新冠疫情长期化的可能性下,新冠药物治疗成为抵抗疫情的最后一道防线。通过有效的治疗可以延缓疾病进程,显著缩短病程,有效改善疾病转归。在新冠肺炎的防治中,新冠药物治疗与疫苗预防形成有效补充,两者缺一不可。
自疫情发生以来,针对新冠药物的开发就一直在持续进行中。当下,赛道已经聚集了众多玩家,而目前市场上较为关注的新冠药物,主要是腾盛博药、再生元、VIR、礼来/君实生物、阿斯利康等知名创新药企联合或单独开发的产品,由于产品技术的差异,不同的药品在针对不同的变异病毒时,表现并不相同,部分抗体并未对所有变异病毒都有效。
而其中最值得注意的是,8月25日,腾盛博药发布公吿,其针对新冠病毒BRII-196/BRII-198联合疗法的ACTIV-2试验III期研究获得积极数据,这也使该药物成为目前国内唯一完成国际临床III期试验的新冠中和抗体药物。
临床III期试验获积极数据,腾盛博药新冠药物进展神速
这次腾盛博药公布试验III期研究获得积极数据距其8月5日宣布ACTIV-2 III期研究完成846位受试者的入组工作仅过去20天。据推算,在短短不到20个月里,公司已经完成了从早期抗体筛选到临床III期试验中期分析已获得积极数据的阶段,可见公司在此项目上进展颇为迅速,这也是市场对其较为关注的原因之一。除研发进展快速外,公司的新冠药物在临床III期的各项数据上,对比当前市场的同类产品,也十分具有竞争力。
在ACTIV-2试验的中期分析中,公司用于治疗新冠肺炎病毒(COVID-19)的中和单克隆抗体BRII-196/BRII-198联合疗法,在837例高风险的新冠肺炎门诊患者中,与安慰剂组相比,住院及死亡的可能性降低78%,相对危险度(RR):0.22(95%置信区间:0.05,0.86),p<0.00001(未调整,单侧检验),具有统计学显著性。
值得注意的是,此次试验是对837例出现症状后10天内入组的高风险门诊患者(年龄≥60岁或任何年龄伴有其他疾病)进行评估。由于越早用药越容易看到药物的抗病毒效果,因此相比于同类型企业针对3天、5天、7天内出现症状的受试者用药,腾盛博药此次试验的难度更高,其住院及死亡的复合终点降低78%,该数据显得含金量更高。
图表一:目前主流新冠中和抗体药物临床III期数据概览
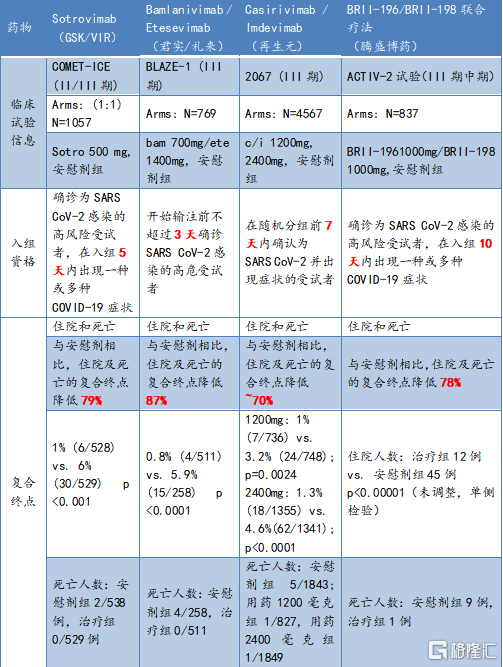
资料来源:公开数据,格隆汇整理
备注:此为翻译版本
目前的体外嵌合病毒实验数据表明,BRII-196/BRII-198联合疗法对广受关注的主要SARS-CoV-2变异株(包括以下常见病毒变异株:B.1.1.7(阿尔法(Alpha))、B.1.351(贝塔(Beta))、P.1(伽马(Gamma))、B.1.429(伊普西龙(Epsilon))、B.1.617.2(德尔塔(Delta))及C.37(拉姆达(Lambda)))均保持中和活性。
赛道齐聚众多玩家,针对变异病毒中和活性成关键
目前全球已进入“第三轮疫情的早期阶段”,而第三轮疫情主要受Delta变异毒株的传播驱动,Delta变异毒株传播能力远远高于原始毒株。而随着疫情的不断发展,未来出现新的变异毒株的可能性不断增大,对新冠药物的要求也不断提高,能否对已出现的变异病毒保持中和抗体活性,成为评价药物优秀与否的关键指标。
而当前备受关注的各个药物此方面表现各异,因而,寻找其中最具投资价值的药物,成为了投资的一大关键因素。
1、再生元——中和抗体 Casirivimab/Imdevimab 联合疗法
再生元的鸡尾酒疗法(Casirivimab(REGN10933)/Imdevimab(REGN10987))是首个获美国EUA的轻中度新冠肺炎抗体鸡尾酒疗法,于2020年11月获批。
其2021年6月临床III期试验达到主要终点,数据显示该药物能提高对新冠病毒缺乏免疫反应的住院患者的生存率,有效减少非入院病人体内病毒水平,降低76%发展为重症的风险。在英国进行临床III期试验显示能降低20%新冠入院病人的死亡率,同时阴性受试者中能减少81%的症状性感染。
据国际权威学术期刊《自然》(Nature)期刊上的研究(《Reduced Sensitivity of SARS-CoV-2 Variant Delta to Antibody Neutralization》)显示,Imdevimab对于多个新冠变种表现出较好的中和能力,而Casirivimab虽然对其它几种病毒株有着比Imdevimab更高的中和能力,但是对Beta病毒株的中和活性表现欠佳(图表二)。
图表二:Casirivimab/Imdevimab针对不同变异病株中和活性表现情况
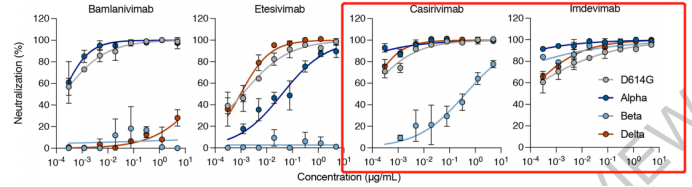
资料来源:《Reduced sensitivity of SARS-CoV-2 variant Delta to antibody neutralization》,格隆汇整理
而在另一知名期刊《BioRxiv》近期发表的文章《Spike mutations in SARS-CoV-2 variants confer resistance to antibody neutralization》中则显示,再生元已被批准用于 EUA 的REGN 10933、REGN 10987,在针对现有变异病株时,其中和活性均受到了不同程度的影响。数据表明,REGN 10933对SA501Y.V2 和BR501Y.V3的 IC 50分别下降13.0倍和8.2倍(图表三)。
同时,此研究中还表明由礼来开发的单抗CB6在针对变异病毒时,受影响较大,其对SA501Y.V2 和BR501Y.V3的IC50因为过低而不在检测区间内(图表三)。
图表三:不同抗体针对不同变异病株中和活性表现情况

资料来源:《Spike mutations in SARS-CoV-2 variants confer resistance to antibody neutralization》,格隆汇整理
2、GSK/Vir Biotechnology—中和抗体 Sotrovimab
由VIR 和 GSK 合作开发的全人源新冠病毒中和抗体——Sotrovimab(VIR-7831)是基于S309抗体开发的单克隆抗体,已于2021年5月获批上市。
临床数据表明,该中和抗体在针对轻中症、非住院新冠患者的临床III期试验中,在主要研究终点全因住院/死亡的受试者比例方面,Sotrovimab组的291名受试者中有3例(1%)报吿了住院或死亡,安慰剂组292名受试者中有21例(7%)患者(P=0.002),相比较下接受Sotrovimab治疗的患者全因住院/死亡绝对减少6%,相对减少85%。
同时有研究(《Antibody Resistance of SARS-CoV-2 Variants B.1.351 and B.1.1.7》)表明,针对B.1.351(Beta),该中和抗体同样表现出了良好的中和活性,针对B.1.1.7(Alpha),S309的中和活性表现不如对照组(图表四)。
图表四:S309针对B.1.351和B.1.1.7的中和活性概况
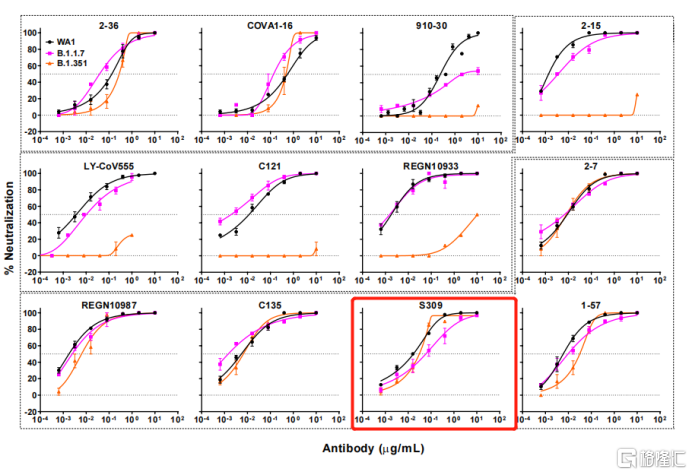
资料来源:《Antibody Resistance of SARS-CoV-2 Variants B.1.351 and B.1.1.7》,格隆汇整理
3、礼来/君实生物——中和抗体 Bamlanivimab/Etesevimab 联合疗法
Bamlanivimab(LY-CoV555)是一种针对SARS-CoV-2棘突蛋白的强效、中和性IgG1单克隆抗体,源自于礼来与AbCellera为预防和治疗COVID-19而进行的研究合作。Etesevimab(JS016或LY-CoV016)是一款重组全人源单克隆中和抗体,由君实生物和中国科学院微生物研究所(IMCAS)在新冠疫情爆发之初共同开发,是中国首个进入临床阶段的中和抗体药物。
2020年5月,双方达成合作授权,礼来从君实生物引进Etesevimab。并于2021年2月10日,获得FDA批准Etesevimab 1400mg和Bamlanivimab 700mg双抗体疗法的紧急使用授权(EUA),用于治疗12岁及以上具有重度或住院高风险的轻中度COVID-19患者。
图表五:Etesevimab针对不同变异病株中和活性表现情况

资料来源:《Reduced sensitivity of SARS-CoV-2 variant Delta to antibody neutralization》,格隆汇整理
值得注意的是,在前文提到的研究中表明,Etesevimab针对Delta病毒表现出了良好的中和活性(图表五)。
4、腾盛博药——中和抗体BRII-196/BRII-198联合疗法
BRII-196和BRII-198为腾盛博药自主研发的抗COVID-19病毒药物,是其在2020年初,与清华大学和深圳市第三人民医院共同成立腾盛华创,并从新冠恢复期患者血清中分离获得的非竞争性新冠病毒中和抗体。
该中和抗体特别应用了基因工程技术以降低抗体介导依赖性增强作用的风险,以及延长血浆半衰期以获得可能更持久的治疗效果。它们的非重叠表位结合区提供了针对SARS-CoV-2的高度中和活性。
早前,在《BioRxiv》 发表的文章(《Antibody Resistance of SARS-CoV-2 Variants B.1.351 and B.1.1.7》)已提到,腾盛博药的联合疗法针对B.1.351 和 B.1.1.7病毒具有良好的中和活性(图表六)。
图表六:BRII-196/BRII-198针对B.1.351 和 B.1.1.7中和活性表现概况
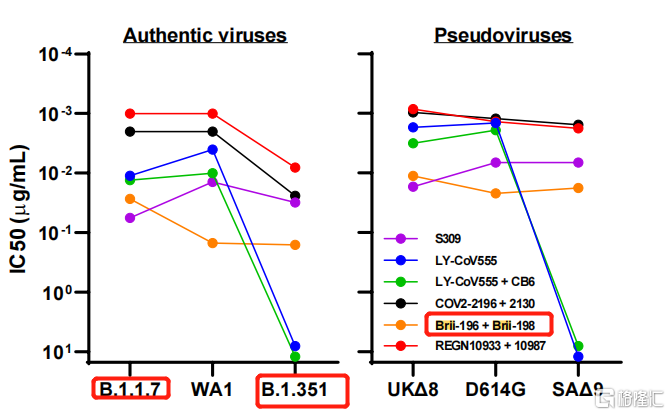
资料来源:《Antibody Resistance of SARS-CoV-2 Variants B.1.351 and B.1.1.7》,格隆汇整理
而在目前最新公布的体外嵌合病毒实验数据表明,BRII-196/BRII-198联合疗法对广受关注的主要SARS-CoV-2变异株均保持中和活性(包括Alpha、Beta、Gamma、Epsilon、Delta及Lambda)。
小结
结合众多专业学术期刊的研究分析和已公布的临床数据来看,腾盛博药的新冠中和抗体药物综合表现出色。
从各研究数据来看,相比于其他药物针对部分变异病毒存在中和活性欠佳的情况,腾盛博药的联合疗法在体外嵌合病毒实验中,针对目前包括传染性较强的Delta病毒在内的主流变异病毒,均表现出了良好的中和活性。
从临床数据来看,腾盛博药的联合疗法在要求更高的临床实验中,表现出了同样优秀的结果,更能显现其相对优势。
由于病毒变异难以预测,因此未来新冠药物在关注研发进度的同时,更要关注其针对不同变异病毒的表现情况。尽管腾盛博药的新冠药物尚未上市,但凭借其优异的表现,一旦上市或将在未来快速实现弯道超车。




