自身免疫疾病藥物市場,是腫瘤之後,全球排名第二的大類醫藥市場,年需求規模接近8000億人民幣,且仍將以超過3%的年複合增速發展。中國的市場規模也超過200億人民幣,但年複合增速預計達到26%,大幅領先全球增速,是一個正快速增長的藍海市場。
近期,專注於自身免疫和腫瘤治療領域,並進行差異化靶點佈局的康諾亞發佈了其2021年上半年業績公吿。
當中,又有什麼值得關注的地方?
1
加大研發,商業化可期
因為產品均處於臨牀研發階段,康諾亞尚無營收,中報主要披露研發、行政方面的開支。
其中,研發費用由去年同期的3993.7萬元增長至1.91億元,行政開支由767.9萬元增長至2683.6萬元;全面虧損總額為36.3億元,當中有34億元是因為首次公開發售,可轉換可贖回優先股公允價值變動所產生,為非現金和非經常性,調整後金額變為1.31億元。
圖表一:公司財務摘要
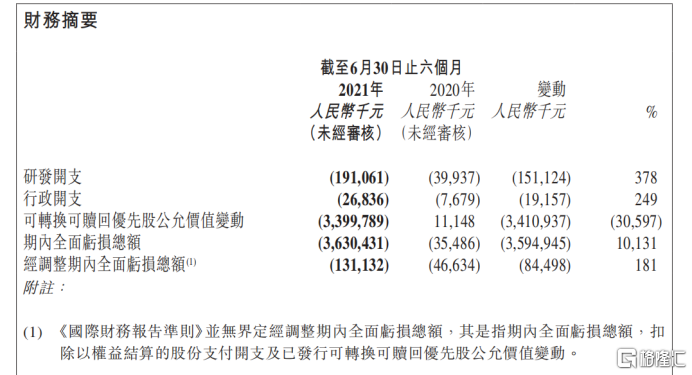
資料來源:公司公吿,格隆彙整理
生物醫藥公司,研發費用是重點。
上半年,康諾亞在研發方面花了1.91億,同比大增378%,從研發管線看,康諾亞有十種可進入臨牀試驗申請及臨牀階段的候選藥物處於內部研發階段,其中五種處於臨牀階段,兩種已向國家藥監局提交臨牀試驗申請並獲受理。其中,CM310有2項適應症推進到臨牀Ⅱ期。
圖表二:公司管線概覽
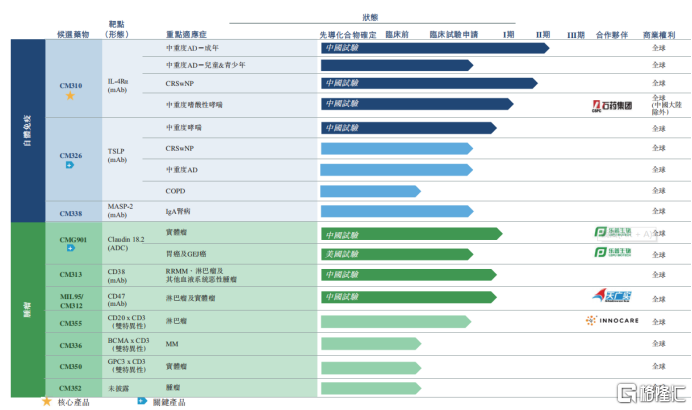
資料來源:公司公吿,格隆彙整理
中報顯示,用於治療成年人中重度特應性皮炎的CM310,有望明年上半年啟動Ⅲ期臨牀,2023年提交上市申請;而CM310的另一個適應症慢性鼻竇炎伴鼻息肉的研發有望在明年上半年進入Ⅲ期臨牀,公司的商業化前景正變得越來越清晰。
圖表三:部分藥物近期進展及未來里程碑事件
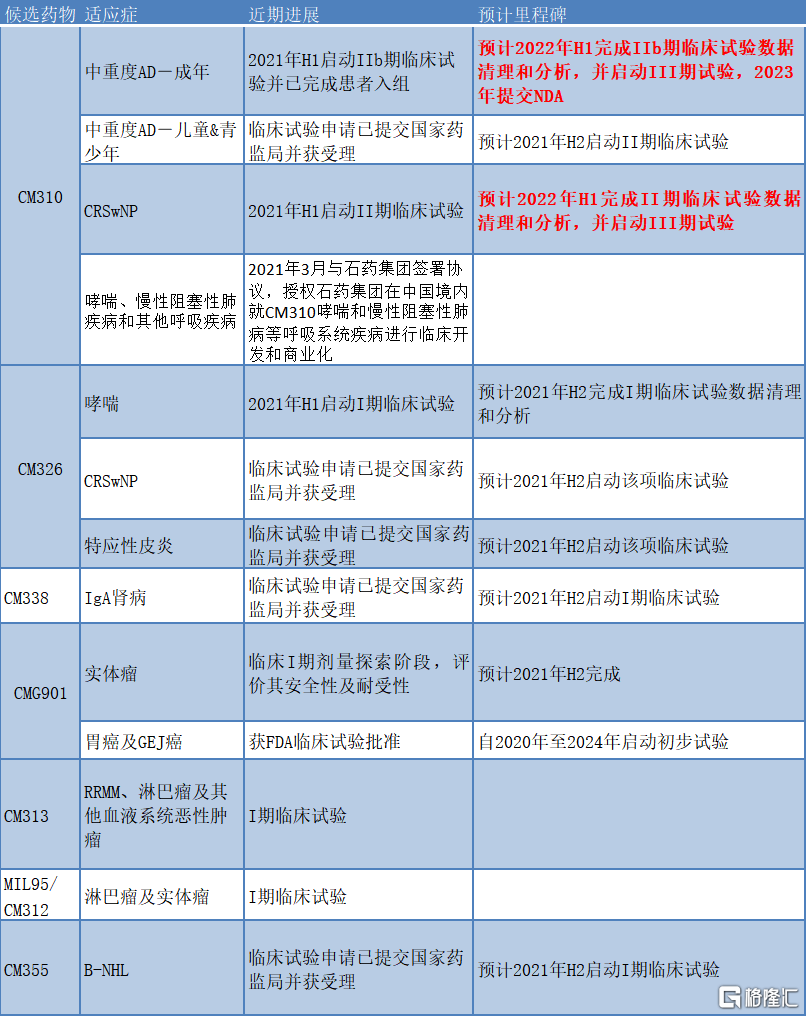
資料來源:公司公吿,格隆彙整理
除了自身免疫,在腫瘤領域的研發也取得新進展,用於治療復發或難治性非霍奇金淋巴瘤(NHL)的CM355的臨牀試驗申請,已提交國家藥監局並獲受理。
2
硬實力如何?
説到生物醫藥公司的投資邏輯,離不開三點,一是研發上,靶點的選擇獨具慧眼,避開過熱競爭,又不失市場需求,並有能力研發出來;二是要具備生產能力;三是有市場推廣和銷售能力。而其中第一點尤為重要。
在重要靶點的選擇上,康諾亞並沒有選擇過度擁擠的PD-1、TNF-α,而是選擇了IL-4Rα、CD47。IL-4Rα能夠雙重阻斷白介素4 (IL-4)及白介素13 (IL-13)兩種關鍵細胞因子的信號傳導,從而治療由它們引發的II型炎症,如中重度特應性皮炎、中重度嗜酸性哮喘,並有望治療慢性阻塞性肺病;而另一靶點CD47,則最有希望成為新的免疫腫瘤靶點之一,通過干擾巨噬細胞上的信號調節蛋白α(SIRPα)受體對CD47的識別,從而阻斷癌細胞的逃逸,使得機體能夠自動殺滅癌細胞。
其中,康諾亞為IL-4Rα國內首個獲批臨牀試驗的公司,也是國內最早進入CD47靶點研究的公司之一。而其他靶點,針對胸腺基質淋巴細胞生成素(TSLP)為中國首個、全世界第三個獲批臨牀試驗;Claudin 18.2抗體偶聯藥物為首個在中國及美國獲批臨牀試驗;CD38是中國首款獲批臨牀試驗;還有治療復發╱難治性非霍奇金淋巴瘤(NHL)的雙抗CD20xCD3。
生物醫藥的研發,搶的就是時間,誰能最快研發出來,誰就最有希望獲得市場增量。在靶點選擇上,康諾亞聚焦於自身免疫、腫瘤治療較為前沿的領域,顯示出走差異化路線的能力,同時也是較早參與到這些領域的公司。
創始團隊中,有國內外領導開發PD-1的研發專家;研發平台上,有創新抗體發現平台、新型T細胞重定向(nTCE)雙特異性抗體平台、生物評估平台、高通量篩選高產抗體藥物表達細胞平台,擁有獨立完成從藥物發現到臨牀前研究,到臨牀開發再到NDA/BLA申請,整個藥物開發流程的專業知識及業務能力。
在生產上,康諾亞擁有1600L、符合中國和美國cGMP標準的產能,今年年初在成都獲批113畝土地,計劃總投資超70億元,建成後將成為西部最大的創新藥物研發及轉化中心,提供超過7萬升產能,其中一期建設產能16000L,先行為商業化鋪路。
圖表四:公司基地概念圖

資料來源:公司官網,格隆彙整理
在籌備後期管線產品的商業化方面,公司也取得進展,與石藥集團簽署協議,授權石藥集團在中國境內就CM310的哮喘和慢阻肺等呼吸疾病領域進行臨牀開發和商業化。
3
結語
港股自開放生物醫藥公司上市以來,生物醫藥一直是熱門的投資賽道。市場最為關注的,無疑是每家生物醫藥的研發進度以及後續的商業化進展情況,研發進展理想,最後成功獲批上市的公司,商業化前景和市場前景就會明朗化。
回到康諾亞,生物藥企的三大核心--研發、生產和銷售(授權合作),實力都不錯,成功登陸資本市場,研發資金上也有所保障。而隨着研發進展的不斷推進,商業化正一步步走來,生物藥企的翻倍神話,看來並不是沒有可能。




