近期,新冠疫情全球多國反覆,根據WIND最新統計數據顯示,截至8月5日,全球累計新冠確診病例超過2億例,累計死亡病例超過427萬例。其中美國累計確診病例超過3630萬例,累計死亡病例超63萬例,美國是累計新冠確診病例和死亡病例最多的國家。
美國佐治亞大學公共衞生學院衞生政策與管理系副教授陳茁8月3日在接受新華社記者採訪時表示,感染病例大多是由德爾塔(Delta)毒株所致。根據美疾控中心公佈的疫情新數據顯示,在7月的最後兩週內,德爾塔毒株感染病例已佔全美新增新冠確診病例的93.4%。另一方面,經WHO確認,全球確診和死亡病例上升主要由德爾塔病毒引起,目前已經有至少132個國家與地區發現了德爾塔毒株。
在中國方面,據國家衞健委通報,國內出現多起由輸入型病例引起的散發病例,多地機場、口岸、定點醫院陸續出現境外輸入關聯病例,並造成一定範圍擴散。截至8月4日9時,有17個省份報吿現有本土確診病例或無症狀感染者,全國中高風險區達144個,為常態化防控以來最多。
德爾塔毒株傳播速度更快、病毒載量更高,但不改本質
上海市新冠肺炎臨牀救治專家組組長張文宏在8月4日的上海市疫情防控工作新聞發佈會上 曾對德爾塔毒株評價為“這個病毒傳播速度比較快,潛伏期比較長,病毒載量比較高”。國內外公共衞生專家也就德爾塔毒株達成共識,認為它複製速度非常快,病毒載量較高,潛伏期較長,因而可以實現快速傳播,在全球快速蔓延。
近期權威期刊nature上刊登了一篇名為《Reduced sensitivity of SARS-CoV-2 variant Delta to antibody neutralization》的論文,認為德爾塔毒株與野生毒株仍有較大的共性,存量疫苗仍能起到一定的中和作用。

JS016被證對德爾塔毒株有效
然而並不是所有的存量疫苗都能對德爾塔毒株起到與原有一樣良好的作用。另一則刊登在國際權威學術期刊《細胞》(Cell)期刊上的研究(《Reduced neutralization of SARS-CoV-2 B.1.617by vaccine and convalescent serum》)認為,則顯示不同廠商的藥物對德爾塔毒株中和能力有所不同。
目前,有許多有效的單克隆抗體正在開發用於臨牀試驗,其中一部分已經獲得緊急使用授權。其中,君實生物海外市場合作夥伴禮來製藥(Lily)的雙抗體療法(LY-CoV555+JS016)針對B.1.617.1及B.1.617.2突變型(最早於印度確認)進行了中和試驗,均證實具有良好的中和活性,針對德爾塔(Delta)毒株有效。

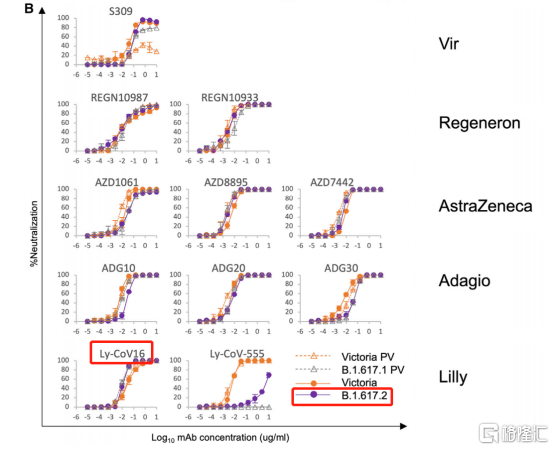
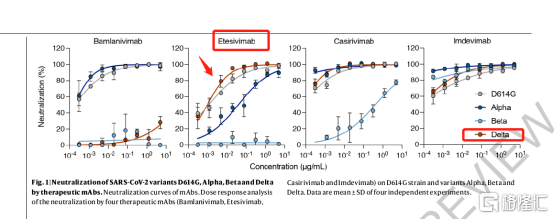
國內本土創新藥企君實生物與中國科學院微生物研究所合作開發的靶向新冠病毒S蛋白的中和抗體JS016(埃特司韋單抗,etesevimab),從2020年疫情爆發初期開始研發到進入臨牀僅用時4個月,於2020年6月作為全球首個在健康志願者中開展的中和抗體,在中國和美國啟動臨牀試驗。針對新冠患者的海外II/III期臨牀已取得積極結果,獲國際高分權威期刊《JAMA》、《新英格蘭醫學雜誌》刊登。如此快速推進入臨牀研究,與其完善的抗體研發與生產平台分割不開。君實生物採用平台化單克隆抗體生產工藝,能夠有效縮減開發時間,具有高質量、高表達、高純度和高收率的特點。
目前,這款中國研發的新冠治療藥物已在歐洲、美國、亞洲、非洲的多個國家投入使用。
2021年2月10日,JS016與另一款海外合作伙伴開發的抗體組成“雙抗體療法”,在美國獲得緊急使用授權(EUA),並獲得美國國立衞生研究院(NIH)推薦。同時,美國FDA批准雙抗體療法輸注時間縮短至21分鐘,大大減輕醫療系統負擔。2月26日,美國政府部門決定採購至少10萬劑雙抗體療法用藥。
今年2月,意大利藥品監管局(AIFA)發文同意了JS016雙抗體療法的緊急使用。緊接着今年3月,歐洲藥品管理局(EMA)人用藥品委員會(CHMP)給予積極科學意見,相當於得到了歐盟層面的特殊授權。此外,今年5月和6月,巴西、印度也相繼公開表示准予雙抗體療法在本國獲得授權使用。
8月5日,埃及衞生部長Hala Zayed在內閣會議上表示,已簽訂相關協議用於獲得JS016雙抗體藥物,這些藥物將很快運達埃及,並被添加到埃及衞生部的治療方案中。Zayed提到,埃及參與了一項WHO世衞開展的臨牀研究,結果證明這一雙抗體療法可有效治療輕度和中度新冠病例,包括緩解了需要將冠狀病毒患者轉移到醫院進行治療的併發症,並減少了死亡人數。目前,埃及在COVID-19傳播水平地圖上排名第二,這意味着該國處於大流行傳播的中等風險。
在全球疫情形勢依舊嚴峻的當下,與新冠疫苗形成互補的治療性藥物市場需求也逐漸顯現,其中中國企業更是處於領先位置。此次專業學術期刊的數據研究顯示,君實生物的中和抗體療法能夠有效針對新冠變異德爾塔毒株,對為其後續的臨牀使用提供了依據,可以預見該藥物將在全球更多國家投入使用。




