2021年7月28日,歌禮制藥公佈了ASC22(恩沃利單抗)聯合核苷(酸)類似物臨牀試驗的最新進展。公吿顯示,首個皮下注射PD-L1抗體ASC22治療慢性乙型肝炎取得良好結果,為開創使用PD-L1抗體治療慢性乙型肝炎的免疫療法邁出了堅實的一步。試驗的順利進展,為ASC22後續的III期臨牀試驗奠定了基礎,也是實現慢性乙型肝炎功能性治癒的重大進展。
慢性乙型肝炎:患者基數大、危害嚴重
乙型病毒性肝炎簡稱乙肝,是由乙肝病毒(HBV)引起的傳染性疾病,有慢性和急性之分。全世界慢性乙肝病毒感染者數量十分龐大,據世界衞生組織《2017年全球肝炎報吿》顯示[1],全球範圍內約有2.57億慢性HBV感染者。在中國約有7000萬慢性HBV感染者,其中慢性乙型肝炎患者約2000萬-3000萬例[2]。慢性乙型肝炎因發病率高、傳染性強、預後差、治癒困難,且長期併發症包括肝硬化、肝功能衰竭和肝細胞癌等,已成為一個重要公共衞生問題。
圖一:全球慢性乙肝感染地圖[3]
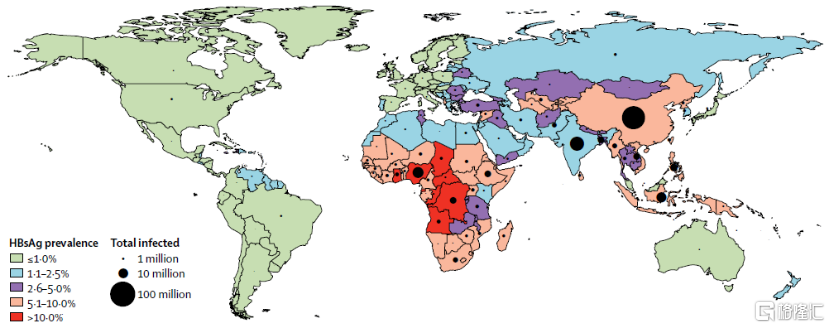
我國已經批准核苷(酸)類似物、Peg-IFN-α和干擾素-α用於治療慢性乙型肝炎患者。雖然能夠有效抑制病毒複製,這些藥物仍面臨HBsAg清除率低等問題,難以實現臨牀治癒(功能性治癒)。所以説,新技術、新靶點、新療法和新長效劑型的產生將是攻克乙型肝炎這個難題的關鍵。
ASC22聯合核苷(酸)類似物:療效和安全性良好
ASC22 IIb期研究是一項在中國進行的隨機、單盲、安慰劑對照的多中心臨牀試驗。試驗療程為24周,採用1 mg/kg或2.5 mg/kg ASC22或安慰劑,每2周給藥1次,聯合核苷(酸)類似物,旨在評估在乙肝表面抗原(HBsAg)<10,000 IU/mL、HBV DNA<20 IU/mL且e抗原(HBeAg)陰性的慢性乙型肝炎患者中的安全性和有效性。
據7月28日公吿,ASC22每2周給藥1次,在1mg/kg劑量聯合核苷(酸)類似物組中,觀察到乙肝表面抗原下降,其中在基線乙肝表面抗原≤500IU/mL的患者中降幅更明顯,在安慰劑聯合核苷(酸)類似物組中未觀察到乙肝表面抗原下降。在1mg/kg和2.5 mg/kg劑量給藥1個月後,預測的受體佔有率仍>90%,表明ASC22有望實現每月給藥1次。
使用1 mg/kg ASC22聯合核苷(酸)類似物治療的患者,其不良事件發生率與安慰劑聯合核苷酸類似物治療的患者相當。2.5mg/kg ASC22聯合核苷(酸)類似物在慢性乙型肝炎患者中安全性與耐受性良好。
持續專注研發、戰略合作促發展
對於一家生物科技公司而言,研發能力的重要性不言而喻,而藥品商業化更是至關重要的一環。歌禮制藥以滿足國內外患者臨牀需求為目標,深耕脂肪性肝炎、腫瘤、病毒性肝炎和艾滋病四大疾病領域,擁有具備深厚專業知識及優秀過往成就的管理和研發團隊。經過多年的發展,歌禮制藥已成為一體化平台型公司,涵蓋了從新藥發現和開發直到生產和商業化的完整價值鏈。
在戰略合作方面,歌禮制藥更是富有遠見。早在2019年1月14日,公司就宣佈與蘇州康寧傑瑞達成了乙肝及其它病毒疾病領域的戰略合作協議。歌禮制藥獲得ASC22在大中華區用於病毒性疾病治療包括乙型肝炎和艾滋病在內的開發和商業化的獨家權益,並有權分享全球除大中華區以外用於病毒性疾病治療的一定收益,包括首付款、里程碑付款及銷售分成。顯然,這份戰略合作協議無疑是對歌禮制藥未來商業化ASC22的一大助力,一旦ASC22成功商業化,將為公司帶來可觀的現金流。
結語
在中國IIb期乙肝試驗中,歌禮制藥的皮下注射PD-L1抗體ASC22取得了良好的中期結果,這也彰顯了公司的研發能力。公司研發進度的順利推動,不僅將為慢性乙肝患者提供給藥方式便捷、療效顯著、安全性好的治療方案,還通過優秀的臨牀數據給予了投資者極大的信心。公司憑藉前瞻性的產品佈局、強大的研發能力、有利的戰略合作等優勢,未來將研發並商業化一個個有價值的產品,為患者治癒疾病的同時也增厚公司的利潤。
參考文獻
[1]WHO. GLOBAL HEPATITIS REPORT,2017.
[2]中華醫學會感染病學分會, 中華醫學會肝病學分會. 慢性乙型肝炎防治指南(2019年版)[J]. 臨牀肝膽病雜誌, 2019, 35(12): 2648-69. DOI: 10.3760/cma.j.issn.1007-3418.2019.12.007.
[3]Polaris Observatory Collaborators. Global prevalence, treatment, and prevention of hepatitis B virus infection in 2016: a modelling study [J]. The lancet Gastroenterology & hepatology 2018, 3(6): 383-403. DOI: 10.1016/s2468-1253(18)30056-6.




