近來,新冠疫情呈現出反撲之勢,而美國是目前全球新冠肺炎確診和死亡病例最多的國家,目前累計新冠肺炎確診病例已經超過4095萬例,其中德爾塔變異毒株佔比較高。據美國廣播公司11日報道,現在全美因新冠肺炎入院的患者人數已超過十萬。此外,開學季之後,兒童感染病例也呈現上升之勢,而隨着秋冬季的到來,疫情的控制難度或將進一步加劇。
美國德爾塔病毒肆虐,疫苗和治療藥物成防治關鍵
然而就在德爾塔變異毒株肆虐美國之際,還有近8000萬美國人沒有接種過新冠疫苗。據美國疾病控制和預防中心(CDC)10日發佈一份報吿稱,未接種新冠疫苗的美國人被感染的可能性是完成疫苗接種者的4.5倍,住院的可能性是接種疫苗者的10倍,死於新冠肺炎的可能性是接種疫苗者的11倍。
在CDC公佈該研究結果的前一天,美國總統拜登在白宮宣佈其“六步走”抗疫新計劃。拜登9日表示,所有員工超過100人的企業,都必須接種疫苗或每週進行新冠檢測。在計劃中,拜登還表示,在已經分發了超過140萬新冠治療藥物的基礎上,從9日起將把該免費的單克隆抗體在全國的貨運速度提高50%,以挽救患者生命和減輕醫院負擔。
圖表一:拜登“六步走”計劃節選

資料來源:CNN,格隆彙整理
其中值得注意的是,此次計劃中所提到的免費的單克隆抗體,所指的正是君實生物和禮來的埃特司韋單抗和巴尼韋單抗(Bamlanivimab/Etesevimab)雙抗體療法,以及再生元的Casirivimab/Imdevimab 聯合療法。
分發加速,君實/禮來雙抗體療法銷量或快速反彈
從投資的角度來看,此次加速新冠單克隆抗體藥物分發速度,或將對當前新冠藥物的市場格局產生一定影響,尤其是君實生物已經獲批上市的JS016產品,更值得關注。
君實生物的JS016是一款重組全人源抗SARS-CoV-2單克隆中和抗體,其能潛在治療和預防COVID-19,是中國首個、全球第二個進入臨牀階段的新冠中和抗體。
在2020年5月全球疫情肆虐之際,君實生物與禮來製藥達成海外合作,組成了埃特司韋單抗和巴尼韋單抗(Bamlanivimab/Etesevimab)雙抗體療法,於2021年2月獲FDA的緊急應用授權,至今已在全球四大洲超過12個國家和地區投入使用。
雖然在今年6月底,美國FDA暫停發放該雙抗體療法。但僅過去兩個月不到,美國疫情病患結構迅速變化。根據美國CDC的統計的數據,2021年8月8日至8月14日間,美國Gamma(P.1)和Beta(B.1.351)變異株總比例僅有0.2%;而佔比最大的突變為Delta(B.1.617.2),佔比86.1%;第二大突變為Delta(AY.3),佔比12.3%。
並且由於多項權威研究表明,該雙抗體療法對目前佔比較高的德爾塔病毒有着較好的療效。9月2日,美國相關衞生部門迅速恢復了雙抗體療法在美國全境的分發。一週後,拜登又明確提出要加快新冠藥物的分發速度,以此減輕醫療系統的負擔。
圖表二:美國新冠病毒突變情況
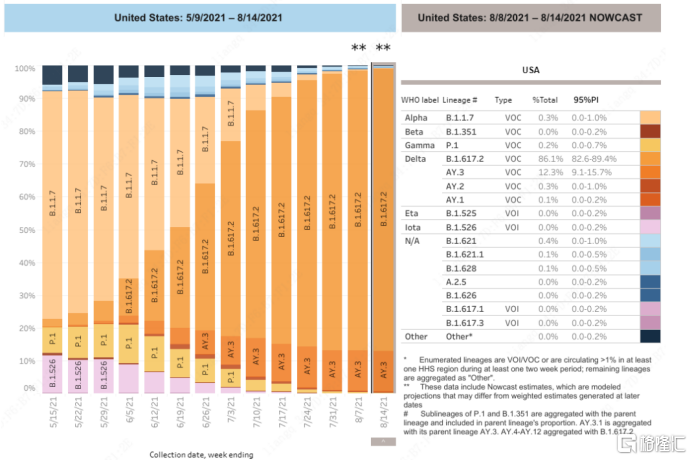
資料來源:美國CDC,格隆彙整理
此次加快分發速度或將快速提升該雙抗體療法的銷售額。從銷售數據上來分析,Bamlanivimab/Etesevimab於2021年2月獲得FDA緊急使用授權(EUA)上市,2021年Q1實現銷售收入8.1億美元,2021年Q2實現銷售收入1.5億美元。
可以看出在獲得EUA後的一季度,其銷售額保持在了較高水平,二季度受暫定分發影響,有所降低。但隨着拜登此次“六步走”政策的施行,該雙抗體療法的銷售額或將快速反彈,同時由於當前美國新冠患者數量仍然十分龐大,因而後續該療法銷售額峯值的出現或將還需要一定時間,未來還有更多價值釋放的空間。
同時,值得注意的是,由於君實生物的JS016存在潛在預防新冠病毒的可能。因而後續不僅僅在新冠治療方面發揮作用,隨着藥物分發範圍和數量的擴大,一旦其潛在預防作用得到臨牀證明,該藥物的需求或將進一步放大。
小結
從行業來看,據不完全統計,目前國內在研治療新冠中和抗體藥物至少有10款,但目前獲批上市的僅有君實生物的JS016,其餘進度較快的也尚處於臨牀III期。並且由於和禮來簽訂了合作協議,其更是在全球市場中強先站穩腳跟,在國際化商業進程方面明顯領先於其他競爭者。
此外,此次拜登“六步走”抗疫計劃加速新冠藥物的分發,為的是不斷加快新冠患者的治療,減少患者數量。對於同賽道的其他競爭者而言,一旦疫情得到有效控制,患者數量不斷減少後,後續獲批的藥物其所能擁有的市場空間或將低於預期。基於此來看,君實生物無疑是當前較為值得關注的標的,其在新冠藥物方面的價值釋放或將領先同業。




