基石藥業-B(2616.HK):重磅產品商業化後首秀成績單,業績與估值共振可期
過去一年多,受新冠疫情的影響,全球經濟雖呈現疲軟態勢,但港股醫療和生物科技領域的IPO依舊十分火熱,去年共有23家醫療健康企業在香港上市,其中包括了康方生物-B(9926.HK)、諾輝健康-B(6606.HK)等在內的多家生物醫藥公司。
而醫藥股一直是資本市場的香餑餑,2020年恆生香港上市生物科技指數上漲49.5%,大幅跑贏恆生指數的-3.7%。這之中,於2019年初在港股上市的基石藥業-B(2616.HK)表現更是尤爲搶眼,從今年3月至6月的短短三個月時間內,股價一度飆漲超120%。
二級市場亮眼表現的背後離不開其重磅新藥上市迎來的商業化,隨着中期財報的到來,也給了我們一個不錯的觀察窗口,進一步探析公司的價值與投資機會。值得一提的是,基石藥業已被納入恆生綜合指數,並於9月6日正式生效。由於恆生綜合指數是港股通樣本基礎,因此,恆生系列指數調整生效後,基石藥業也於生效當日正式納入港股通。
隨着這份中期成績單的出爐,疊加正式納入恆生綜合指數和港股通,並以此帶來市場關注度的擴大以及被動資金的加持等,基石藥業在多重利好催化之下,後續行情走勢將頗爲引人期待。
1、商業化首秀成績亮眼,開啓新一輪估值增長
8月26日晚,基石藥業發佈了2021年中報,公司上半年推出的兩款重磅藥的商業化率先成爲投資人關注的焦點。
財報顯示,兩款上市新品泰吉華®和普吉華®在短短兩個月內銷售業績分別達到3360萬元及4580萬元人民幣。
毫無疑問,公司交出了一份靚麗的商業化首秀成績單,向市場證明瞭基石藥業不僅有着強勁的研發創新能力,在商業化的能力上同樣不容小覷。
在筆者看來,優異的成績背後,公司強大且高效的市場準入能力和商業化效率值得報以十二分的關注。
今年三月最後一天,泰吉華®獲得中國國家藥品監督管理局(NMPA)批準上市,而在5月6日,該款新藥即在北京大學腫瘤醫院、北京大學人民醫院等近三十家醫院同步開出首批處方單,並正式面向全國多個省市的五十多家院內和院外藥房供藥。
而於3月24日獲批的普吉華®,在6月21日就已經在廣東省人民醫院等近百家醫院開出近200張處方單,並面向全國近70個城市約80家藥房供藥。
不論是從產品快速推向市場,還是在取得了理想的銷售業績上,都不難看出基石藥業在商業化上突出的實力。要知道新藥上市往往只是萬裏長徵的第一步,其上市後的商業能力纔是更爲考驗創新藥企的關鍵所在。一方面在於產品是否得到市場的認同,另一方面也在於公司商業化體系的建設能力。從這點來看,基石藥業的成績已經是有目共睹。
俗話說,羅馬不是一日建成的。在兩款藥品面向市場之前,基石藥業就已經做了大量前期準備工作,公司對全國市場進行了加速覆蓋。
截至目前,基石藥業的銷售渠道已經覆蓋了中國超過130個城市的400多家醫院,且其精準治療藥物已覆蓋的醫院佔相關市場約70-80%,已被納入20項主要商業保險及政府保險計劃。
在2021年上半年,基石藥業的商業隊伍人數已從2020年底的200人擴張至300人左右,預計會在2023年擴展到600人左右,將爲後續上市的新藥提供更廣闊的銷售渠道,推動產品實現商業化。
與此同時,爲了助推後續上市的新藥舒格利單抗能在中國大陸更好地實現商業化,基石藥業與輝瑞就舒格利單抗在中國大陸的開發和商業化達成戰略合作,目前輝瑞擁有中國腫瘤銷售團隊規模超1000人,覆蓋超過300個城市和2600多家醫院。此外,輝瑞擁有覆蓋5個治療領域的11個腫瘤藥國家醫保目錄談判的豐富經驗,也有助於舒格利單抗在上市後將其儘快納入醫保,以最大化產品的可及性。
而公司在商業化能力上的突出表現,將爲其帶來更大的市場機會,這也勢必將成爲驅動其在資本市場估值增長的催化劑。隨着重磅藥品上市帶來的強勁業績預期,公司也已經迎來了新一輪估值增長。
2、重磅上市藥品構築市值強力支撐
核心產品投放市場可以說是創新藥企“跨龍門”的驚險一躍,最終展現的成果如何直接將影響到市場的預期。而基石藥業交出的這份財報帶給了市場驚喜,從二級市場的表現來看,近期公司股價亦呈現明顯走強趨勢,體現了市場資金對其給予了積極反饋。
從兩大上市藥品的具體情況來看,差異化的創新路徑以及所佈局的龐大潛力市場,爲後續業績帶來了支撐。
具體而言,公司第一款上市新藥普吉華®(普拉替尼),其在中國申請的適應症是:用於治療經含鉑化療的RET融合陽性的非小細胞肺癌患者。作爲國內第一個針對RET融合陽性的靶向藥,同時針對的又是肺癌這樣的國內患病率第一高癌種,其市場潛力不容置疑。此前人民日報發文,截止2020年,全球新發癌症發病率最高的爲肺癌,而我國每年新增肺癌患者就超過了82萬,相比2019年的78.4萬,僅僅一年增長率就達到了4%。另外,據統計RET融合陽性的中國患者每年新增8萬人。
作爲國內率先跑出的RET抑制劑,普吉華®具有顯著的先發優勢,同時其在拓展適應症上亦顯示出相當大的潛力。在今年4月底,普吉華®用於RET突變MTC和RET融合陽性TC的適應證獲得NMPA受理並被納入優先審評,這比原計劃提前了半年。目前中國RET突變型甲狀腺髓樣癌患者尚無有效的獲批標準治療方案,隨着此次被NMPA納入優先審評這也意味着其有望成爲首個獲批的RET變異甲狀腺癌的精準靶向藥物。而憑藉適應症的廣泛佈局、優越的有效性和首創價值,其市場潛力和價值也將進一步放大。
近年來,越來越多的抗癌藥被納入了醫保範疇。據2020年醫保談判目錄中顯示,去年被納入醫保談判目錄的抗癌藥主要適應症包括黑色素瘤、非小細胞肺癌、霍奇金淋巴瘤、食管癌、肝癌、頭頸部癌等。而近期,國家醫保局最新發布了一份《關於公示2021年國家醫保藥品目錄調整通過初步形式審查藥品及信息的公告》,目前共有271類藥品已經通過了初步審查,這其中合計有58類抗腫瘤藥物在初審名單上,也出現了國產藥品的身影。因此,憑藉着顯著的療效和安全性,普吉華®後續進入醫保也將值得期待。
從第二款新藥泰吉華®(阿伐替尼)來看,雖然其針對的不可切除或轉移性GIST患者羣體數量較少,但是基石切實的考慮到了臨牀的需求,解決這類疾病突變患者此前無藥可用的窘境。這也反映出公司在新藥研發上高度關注患者未被滿足的臨牀需求,兼顧了社會效益與經濟效益。
可以說,研發成果轉化後的商業化使公司價值曲線邁向新的轉折,基於公司兩大創新藥品帶來的業績潛力,公司已經開啓了新的增長模型,商業價值迎來加速釋放。而兩大創新藥品也爲公司的估值提供有力支撐,隨着盈利能力的快速提升,後續業績與估值在資本市場上有望形成共振上行。
3、創新管線加速推進打開估值空間
在新藥對估值支撐的前提下,決定公司估值增量空間的則是需要關注其在研管線所展現的價值。
截至2021年上半年,基石藥業已在多個腫瘤治療領域及相關適應症上建立了成熟管線,並相繼取得了不同程度的突破。
如目前用於治療IDH1突變復發/難治性急性髓系白血病的艾伏尼布已於8月份獲得了國家藥監局的受理並獲得優先評審資格,是國內首個療效明確且安全性良好的IDH1抑制劑。預計會在今年底或明年一季度獲得新藥上市申請(NDA)批準。
另外在8月份,公司合作夥伴施維雅發佈有關艾伏尼布與阿扎胞苷聯合治療未經治療的IDH1突變急性髓系白血病的全球III期研究正面頂線數據,由於療效優異該研究停止進一步入組。
其中特別值得關注的是,公司自主研發的舒格利單抗。作爲一種全人源全長抗PD-L1單克隆抗體,其能夠降低患者的免疫原性及病毒風險,與同類藥物相比,不易引發ILD等副作用,具有更好的安全性優勢。
值得一提的是,9月2日,中國國家藥品監督管理局(NMPA)已正式受理了基石藥業所遞交的舒格利單抗治療局部晚期/不可切除(III期)非小細胞肺癌的新品上市申請;與此同時,舒格利單抗治療轉移性(IV期)非小細胞肺癌的新藥上市申請已於去年獲NMPA受理,目前正在審評中,預期將於今年年底獲批。這意味着舒格利單抗有望成爲全球首個同時覆蓋局部晚期/不可切除(III期)和轉移性(IV期)非小細胞肺癌全人羣的PD-L1單抗。
除了肺癌領域,目前舒格利單抗已進行多項註冊性臨牀試驗,包括一項針對淋巴瘤的II期註冊臨牀試驗(CS1001-201),以及四項分別在III期、IV期非小細胞肺癌、胃癌和食管癌的III期註冊臨牀試驗。與此同時,舒格利單抗聯合fisogatinib(非索替尼)用於不同的適應症的試驗也在順利推進,有望在多種療法上實現突破。
同時可以看到,舒格利單抗在適應症的覆蓋上也做出了不輸羅氏和默沙東等進口產品的成績,其在胃癌、食管癌等多個常見癌種上都有臨牀數據的支持,更好地擴大了其適應症的範圍。
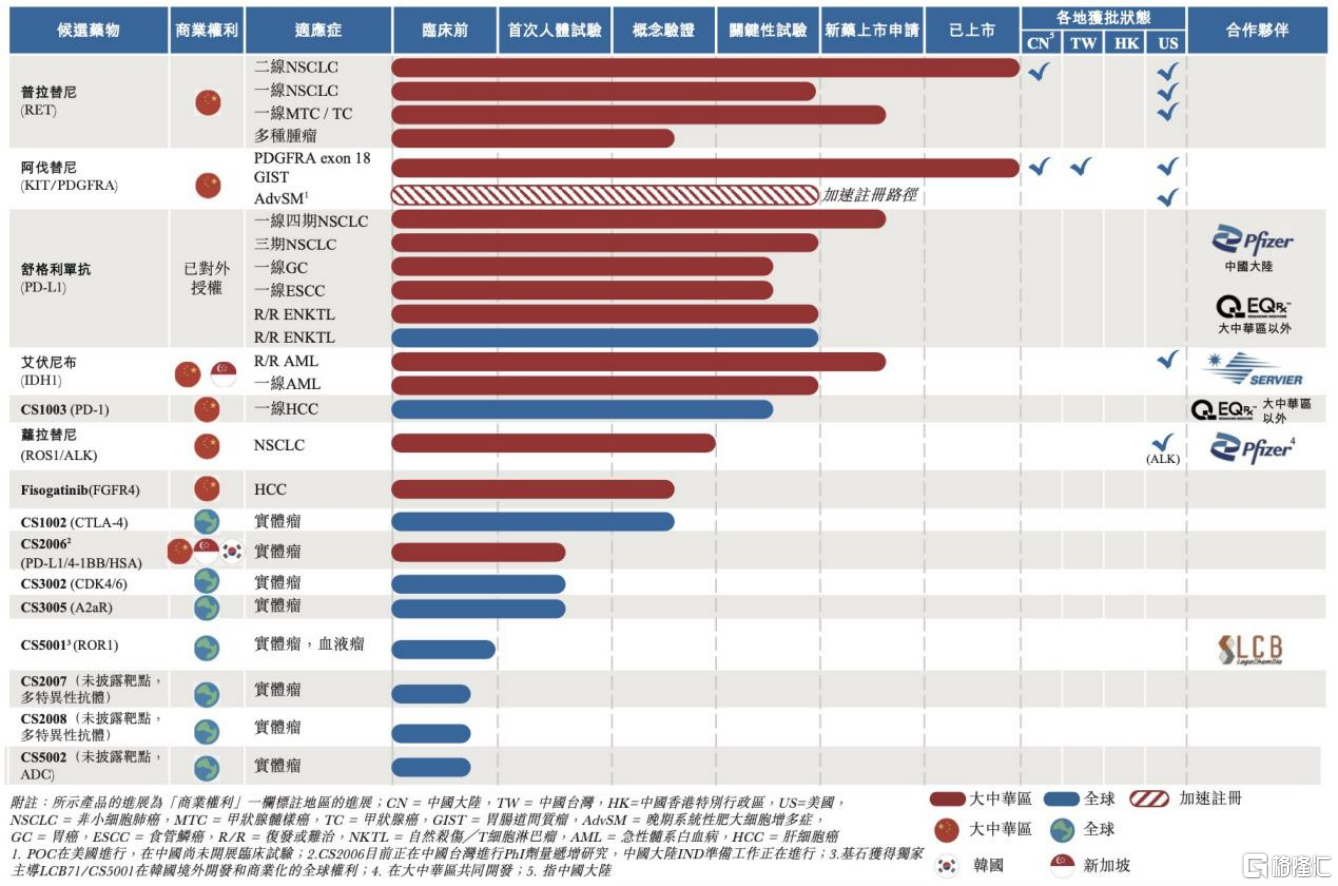
(來源:公司公告)
照此推算,如果基石藥業的PD-L1產品能夠在今年底順利面世,其不僅能爲患者提供更加便利的臨牀治療選擇,把握住國內廣闊的市場前景;同時還能在宏觀層面給公司的產品線注入新的生命力,使公司在肺癌精準治療與免疫治療領域進一步建立起自己的話語權,在行業中佔據絕對優勢。
值得一提的是爲進一步擴大海外市場的藥物適應症試驗範圍,基石藥業還和EQRx共同與美國、英國及歐盟等全球主要市場的利益相關者就舒格利單抗治療非小細胞肺癌適應症的註冊進行洽談,如果產品能夠成功在全球其他國家成功上市,也將進一步擴大公司全球商業化的道路。
在強勁的自主研發實力下,基石藥業亦積極與國際醫藥巨頭展開戰略合作進一步拓展管線。如在今年上半年公司就進一步深化了與輝瑞的合作,針對ROS1陽性晚期非小細胞肺癌開展合作研究,共同開發勞拉替尼。勞拉替尼是輝瑞全球管線中的新一代ALK/ROS1靶向藥物,在國內屬於一款滿足臨牀需求缺口的藥物。此次基石藥業與輝瑞的協力合作不僅可以將新的腫瘤療法引入國內市場,同時也將與國際醫藥巨頭形成更緊密的合作關係,爲未來在研發、商業化等方面的進一步合作奠定基礎。
從公司管線的佈局來看,實際上也可以梳理出公司的優勢特徵,即對具備同類首創(FIC)和同類最優(BIC)第一梯隊潛力的品種進行開發,做出短期內不可替代的新藥。公司以BIC/FIC爲研發的戰略重心,有助於新藥在上市後獲得自主定價權,並以此斬獲更大的市場機會。
所以基石藥業已經上市和未來即將上市的幾款新藥,都朝着FIC或BIC的方向努力,在首創性、獨特性等優勢支撐下,其在臨牀開發上也有望得到諸如優先審評、加速批準和臨牀急需用藥名單等政策助力,取得市場先機。同時這也將賦予其後續業績的持續性和爆發力,併爲其打開估值天花板。
從目前管線進展以及商業化運營情況來看,公司在優異的在研產品佈局以及商業化能力搭建之下,已經形成了一條“上市產品快速放量—驅動盈利提升—反哺創新發展”的循環模式。後續隨着公司更多極具競爭力的新藥陸續獲批上市,無疑也將給其在資本市場的價值帶來新的突破。
4、小結
基石藥業作爲一家生物製藥公司,最重要的護城河就是研發和商業化的能力。從誕生之初,基石藥業就將研發佈局在市場空間最大的腫瘤賽道上,公司專注中國高發癌症,覆蓋五大高發腫瘤,擁有非常廣闊的市場前景。而隨着上半年重磅產品的面世也使得公司的業績表現迎來了新的轉折點,爲後續的研發帶來了強勁源動力。
公司高度重視研發,從中期業績報來看,其中按照非國際財務報告準則計算,扣除以股份爲基礎的付款開支後的研發開支爲4.45億元,該研發費用在同類香港上市公司中排名處在領先位置。
隨着未來更多新藥的獲批上市,公司強勁的研發能力還將不斷得到鞏固。而其打造的具有領先優勢的產品也能推動公司站穩海外市場,憑藉公司強大的商業化能力,進一步助力其在行業內形成一條“不可替代”的獨特發展路徑——以更多適應症覆蓋的優秀新藥搶佔市場份額,保障公司實現商業價值的最大化。
看回以往創新藥研發上市後的走勢,無疑都是這一發展路徑,而擁有多個即將通過NDA的產品的基石藥業相信也將做得更好,隨着公司在今年業績打開全新的上升通道,相信也能推動其在資本市場迎來價值重估。



