近日,美國血液學會(ASH)年會召開,作為全球血液學領域最負盛名的國際學術盛會之一,能夠在ASH年會上發佈臨牀數據的產品無疑都具備顯著的創新性和臨牀應用潛力,同時也反映了企業在創新研發方面的實力。
會上,基石藥業公佈了重磅產品CS5001作為單藥針對晚期淋巴瘤的最新臨牀數據,展現出良好的療效和安全性。作為首個在實體瘤和淋巴瘤中均觀察到臨牀療效的ROR1 ADC,CS5001的亮相快速引起了業內的廣泛關注。
公吿一經發出,基石藥業的股價升幅一度超過7%,可見市場對該產品前景的積極反應。對於投資者而言,這背後或許也隱藏着一個有價值的投資機會。
1、ORR高達76.9%,潛在同類最佳彰顯差異化臨牀價值
從產品結構設計上來看,CS5001作為一種新型ROR1導向的ADC,就已經展現出十足的創新性。吡咯並苯二氮卓(PBD)前藥的獨特設計,賦予了CS5001擁有同類最佳產品潛力的優勢。簡單來説有四大差異化優勢:
其一,全人源抗IgG1抗ROR1抗體因其與人體的高度相容性而減少免疫原性,從而可能降低副作用風險,提高治療安全性;
其二,位點特異性偶聯技術能夠精確控制藥物與抗體的比例達到2,有助於確保藥物的均勻分佈和穩定性,提高療效並減少副作用;
其三,專屬腫瘤選擇性可降解連接子(由β-葡萄糖醛酸酶裂解)意味着其能夠在血液循環系統中保持高度穩定,直到到達腫瘤微環境;
其四,腫瘤微環境中特異性激活PBD二聚體毒素前藥(由β-葡萄糖醛酸酶酶切釋放)能夠通過DNA交聯機制有效殺傷腫瘤細胞,避免腫瘤耐藥性的產生。
基於此,本次CS5001作為單藥針對晚期淋巴瘤最新的積極臨牀數據,也進一步證明了CS5001的安全性和潛在的臨牀應用價值。
於療效性方面,無論患者的ROR1表達水平如何,從最低有效劑量開始,CS5001在晚期霍奇金淋巴瘤(HL)患者中的ORR達到了60.0%,而在非霍奇金淋巴瘤(NHL)患者中的ORR為56.3%。
特別值得一提的是,在初步確定的II期推薦劑量(RP2D)水平——DL8(125 μg/kg)中,晚期B細胞淋巴瘤患者的ORR更是高達76.9%,其中所有可評估的HL患者均實現了完全或部分緩解,NHL患者的ORR也達到了70%。
於安全性方面,CS5001在多線經治的晚期B細胞淋巴瘤患者中,展現出良好的耐受性,且在10個不同劑量組的研究中,沒有報吿任何劑量限制性毒性(DLT)。
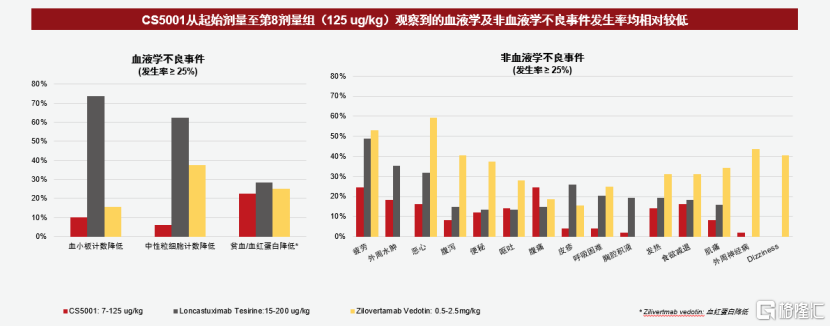
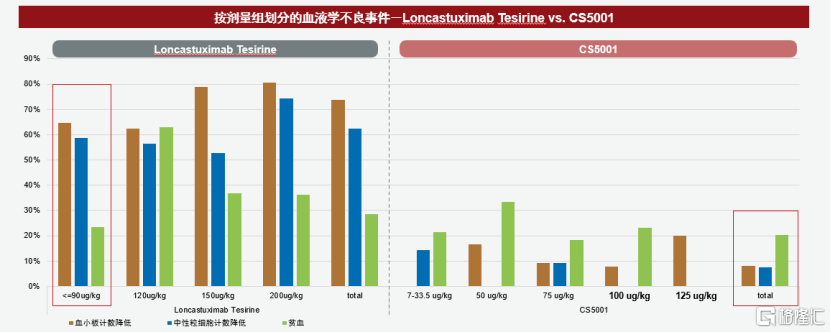
進一步對比市場上已有的兩種相關ADC,CS5001在I期臨牀試驗中的不良事件發生率相對較低。特別是在I期劑量探索研究中,與其他PBD類ADC相比,CS5001也顯示出更低的血液學毒性。
隨着CS5001在臨牀試驗中展現出的積極數據,我們有理由相信,ROR1 ADC藥物有望成為全球晚期淋巴瘤患者治療的重要選擇。
據悉,目前CS5001的全球多中心試驗正在美國、澳大利亞和中國同步進行,劑量遞增階段已經順利完成,該產品的國際化步伐正在穩步推進,並且基石藥業還將於近期啟動涵蓋多瘤種、具有註冊潛力的1b期劑量擴展研究。
可以預見,此次針對晚期淋巴瘤治療的積極結果,也將為CS5001在其他多種實體瘤和血液瘤的探索上提供經驗和數據支撐,展現出更多臨牀應用潛力。
2、手握多款FIC/BIC,增長引擎正在加速轉動
透過CS5001,背後映射出來的則是基石藥業的創新能力。
從管線佈局來看,基石藥業2.0的管線主打差異化競爭,PD-1/VEGFA/CTLA4三抗、EGFR/HER3雙抗及ADC、ITGB4 ADC、SSTR2系列管線,自免雙抗管線等17款候選藥物極具市場潛力,致力於最大化成熟產品的商業價值。

除了此次ASH年會上公佈數據的CS5001外,基石藥業的CS2009也是一大值得關注的亮點。
作為PD-1/VEGFA/CTLA-4三特異性抗體,CS2009獨特的設計有望使其取代現有的PD-(L)1單抗,成為下一代腫瘤免疫治療的骨幹產品,具有成為FIC的潛力,目前即將進入臨牀階段。
最新的臨牀數據顯示,與PD-1/L1單藥治療相比,PD-1/L1聯合VEGFA治療雖然能夠改善無進展生存期(PFS),但在總生存期(OS)上的獲益並不明顯。同時,PD-1/L1聯合CTLA-4治療的長期生存協同作用在最近發表的臨牀數據中得到了證實。
基於這些發現,基石藥業通過將PD-1、VEGFA和CTLA-4三種抗體聯合起來,旨在實現最大的生存獲益。此前,CS2009的臨牀前研究數據就已經顯示出在抗腫瘤活性方面明顯優於潛在的競品,包括PD-1/CTLA-4雙抗和PD-1/VEGFA雙抗。
值得注意的是,基石藥業也是推動中國生物藥國際化的排頭兵,旗下已有3款商業化產品通過合作伙伴在全球市場銷售。此外,首個成功出海的由中國生物製藥企業研發的PD-L1單抗——舒格利單抗目前已獲得在歐盟,歐洲經濟區國家以及英國的上市許可。毫無疑問,這將為基石藥業未來其他產品的上市和國際市場開拓提供有力的支持和快速的放量。
根據今年的中期業績報吿,基石藥業現已開始盈利,進一步印證了其的增長引擎正在良性轉動。強勢的臨牀開發能力結合差異化的產品管線,國內自主開發與全球商業化合作並行,基石藥業已經具備了中國Biotech可持續發展的核心要素。相信隨着公司對創新管線研發的持續深入,會陸續收穫市場價值的回饋。




