6月13日,受美國通脹高企、消費者信心低迷以及美聯儲可能在6月進一步加息的擔憂下,美股遭遇重挫,納斯達克指數跌近4.7%。而向來與美股市場同頻共振的港股市場在次日早間有所下挫後,開啟反彈,走出相對獨立行情,但整體仍然呈微跌趨勢。在大盤略顯低迷的行情中,筆者留意到信達生物(01801.HK)迎來強勢反彈,當日盤中一度大漲5%,而自5月中旬以來公司累計漲幅達到40%,大幅跑贏同期恆指約為5%的升幅表現。
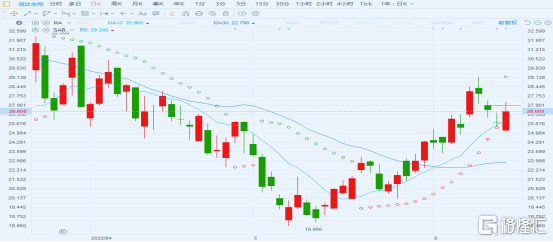
(來源:富途行情)
消息面上來看,信達生物13日晚間及次日早間接連公佈兩項重要公吿,其一,國家藥品監督管理局受理公司託萊西單抗注射液的新藥上市許可申請,其二則是公司達攸同®獲得印尼食品藥品監督管理局(BPOM)批准用於治療轉移性結直腸癌,轉移性三陰性乳腺癌等在內的五項適應症。
下面不妨借這兩個公吿一同來看看市場應聲逆勢而漲的積極響應背後,暗示着公司什麼樣的價值線索?
1、首款國產PCSK9單抗申報上市,打破進口壟斷彰顯硬核創新實力
首先是信達生物遞交1類新藥託萊西單抗注射液的上市申請獲受理,其申報上市適應症應為原發性高膽固醇血癥和混合型血脂異常。作為信達生物開發的一種靶向PCSK9的單克隆抗體,此前在今年2月,信達生物就曾宣佈託萊西單抗順利完成3項關鍵臨牀,開始向上市發起衝刺。

(來自:CDE 官網)
相關資料顯示,目前我國上市PCSK9抑制劑有兩種,分別是依洛尤單抗和阿利西尤單抗,而隨着2022年01月國家醫保目錄的實施,這兩個藥物也已經進入醫保乙類目錄,售價由此前一千多降到目前約300左右。PCSK9抑制劑打破了過去他汀類藥物在高血脂藥物治療領域一枝獨秀的局面,在降脂效果方面強於他汀類藥物,且無需每日服藥。隨着進入醫保大幅降價也進一步提高了可及性、擴大了市場覆蓋。
儘管目前國內仍然有六個同類國產新藥處於在研階段顯示出這一賽道激烈的競爭態勢,不過從信達生物此次獲批所處的階段來看,其既領先於國內一眾藥企並率先打破海外壟斷,同時又處在市場進一步放量的黃金窗口期,後續隨着商業化推進,憑藉本土優勢以及國產先發優勢,公司後在進口替代以及市場擴容上有望持續受益。
此外從這款藥物的開發進程來看,託萊西單抗作為信達自主開發的創新型生物藥,早在2017年初,信達首次就遞交該藥臨牀申請,同年11月啟動臨牀。在經歷短短五年的臨牀開發該藥即迎來了商業化階段,並具備打破進口壟斷的時潛力,這足以見得信達生物強勁的研發實力和執行力。
實際上這一點也充分體現在近年來公司持續推進的新藥管線上。
如在本月初,信達生物就公吿其與馴鹿生物共同開發的伊基侖賽注射液新藥上市申請獲國家藥監局受理。而該注射液是國內第一款全流程自主研發的CAR-T細胞治療產品,也是國內首家遞交新藥上市獲受理並有望成為首款獲批的靶向BCMA的自體嵌合抗原受體T細胞免疫治療產品。
此外同樣是在月初舉辦的2022年美國臨牀腫瘤學會(ASCO)年會上,信達生物公佈了多個創新分子的臨牀研究數據。值得一提的是公司公佈了IBI110(LAG-3單抗)一期臨牀研究的多項數據,作為中國研發進展最快的LAG-3單抗之一,IBI110展現出令人鼓舞的初步療效信號。在非腫瘤管線上,月初信達生物胰高血糖素樣肽-1受體/胰高血糖素受體雙重激動劑mazdutide(研發代號:IBI362)在中國超重或肥胖受試者中的一項隨機、雙盲、安慰劑對照的II期臨牀研究達到了主要臨牀終點和所有的關鍵次要臨牀終點。近日,IBI362肥胖或超重臨牀Ib研究高劑量組數據亮相美國內分泌年會(ENDO 2022),初步數據非常亮眼,信達表示,將在今年下半年開始積極推進IBI362 III期臨牀研究的開展。
從這一系列新藥的進展中,不難看到公司具備開發出具有開創性重磅新藥的核心能力。隨着後續各管線不斷推進,信達生物也將有望進入下一輪的商業化爆發期,業績與成長前景可期。
2、達攸同®獲印尼批准治療五項癌症,國際化進程再進一步
接下來再來看另一份公吿,即達攸同®在印尼獲批多項適應症,這展現了公司在海外商業化佈局上的里程碑式的進展與突破。
據悉在去年1月18日信達生物就曾與印度尼西亞生物科技公司PT Etana Biotechnologies Indonesia (Etana)關於達攸同®簽訂合作協議,公司授予Etana達攸同®在印尼的獨家許可,Etana致力於將達攸同®推向當地市場。而在僅僅一年之後,達攸同®即在印尼傳來好消息,此次獲批不僅意味着信達生物將這一重磅產品帶到印尼,同時其還有望成為第一個在東南亞商業化和本地化生產的中國抗體藥。
當前,伴隨國內醫藥市場加速內卷的大背景下,具備實力的本土藥企積極推進出海進程,信達生物也湧進了這一股潮流中,儘管此前出海美國並不算順利,並一度挫傷市場信心。不過從此次信達在印尼市場的突破來看,公司的出海潛力仍然不容小覷。這次出海新興市場更有助於公司發揮自身優勢實現快速准入,同時憑藉在當地的領先優勢也更有機會在這一市場獲得更高的回報。
印尼作為世界第四人口大國,總人口高達2.62億。而根據GLOBOCAN 2020,印尼每年新發癌症病例中排名前五的癌症分別為,乳腺癌(16.6%),宮頸癌(9.2%),肺癌(8.8%),肝癌(5.4%)以及結直腸癌(4.4%)。此次達攸同®基本獲批了上述大部分癌種的適應症。不難預判,後續公司有望在這一市場獲得強勁的業績驅動力。
展望後續,公司在順利進入到印尼市場後,也將有機會進一步打開東南亞市場,並延伸到更多的海外新興市場之中,其成長潛力也將藉此進一步打開,長期價值持續得到凸顯。強大的研發實力與全球化的合作佈局,是支撐信達生物海外商業化的重要基礎所在,未來公司也有望將更多的藥物推向海外市場,實現破圈,重塑增長曲線。
3、結語
近期,伴隨多重利好加持,信達生物股價走出一波亮眼的反彈,結合專業投資機構的觀點來看,這也絕非只是“曇花一現”,公司長期價值仍然具備穩固支撐。近期包括高盛、麥格理、大摩、招商證券(香港)、瑞銀等接連發布研究報吿看好公司發展。
其中麥格理表示,信達生物近日多項產品的臨牀研究結果出現進展,展示出公司在各個治療領域的研發能力和多樣性。該行根據臨牀研究數據提高對IBI326及IBI362的銷售峯值預測,並將信達生物目標價上調1%至44元,認為產品具有競爭力。
招商證券(香港)則指在中國主要生物科技企業(市值超過5億美元)中,信達生物目前估值更有吸引力(22財年市銷率為5.6倍,同業均值為17倍)。其維持信達生物(01801)“買入”評級,基於分類加總估值法,目標價110港元。
高盛研報則維持信達生物“買入”評級與60.3港元目標價。大摩調升公司目標價,由42.25港元上調至42.5港元,評級維持“增持”。
一眾投資機構的積極表態進一步驗證了公司成長潛力,考慮到當前醫藥板塊整體估值仍處在較低水平,在後續不斷修復的市場行情中,公司優質的基本面也將有望進一步獲得估值溢價,公司在市場的稀缺價值也將持續凸顯。




