本文來自:藥明康德
第三劑新冠疫苗提高中和抗體滴度5-8倍
輝瑞在電話會議上表示,新近出現的Delta變種正在全球範圍內廣泛傳播,而真實世界數據顯示,防止新冠病毒感染或症狀性疾病的免疫力隨着時間的推移可能會減弱。因此,何時進行疫苗增強接種,對哪些人羣進行增強接種,正在成爲監管機構考慮的問題。
輝瑞和BioNTech進行的臨牀試驗的初步數據顯示,在接種第二劑BNT162b2疫苗6個月之後,接種第三劑增強疫苗表現出與此前一致的安全性特徵。
針對野生型病毒,接種第三劑疫苗後中和抗體滴度與接種完第二劑疫苗後相比,提高5-8倍。
針對最初在南非發現的Beta變種(B.1.351),接種第三劑疫苗後,中和抗體滴度與接種完第二劑疫苗後相比,提高15-21倍。
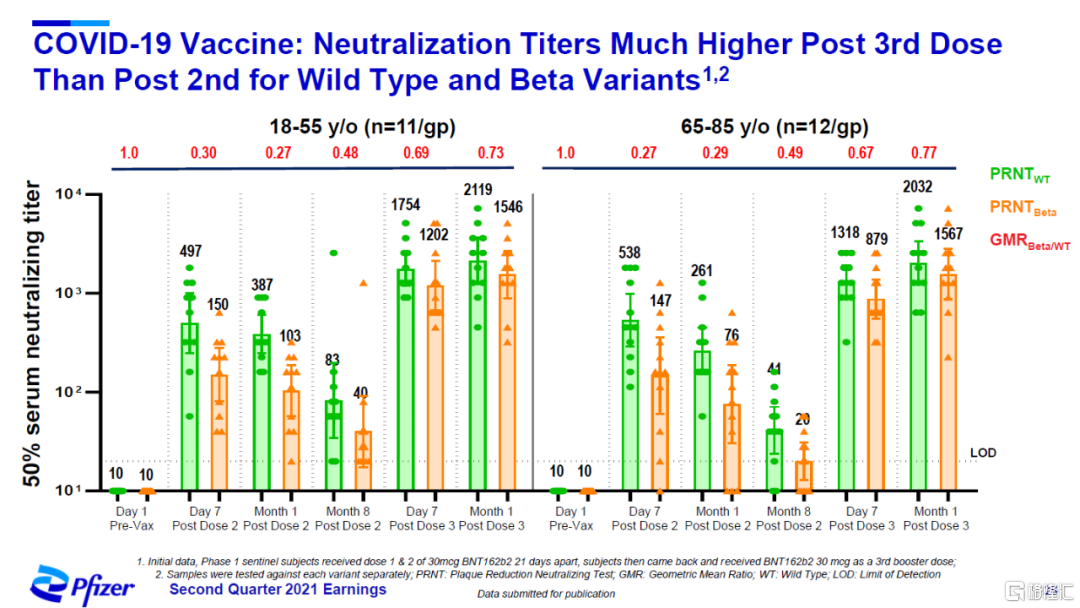
▲接種第三劑疫苗在成人(18-55歲,左圖)和老年人(65-80歲,右圖)羣體中均顯著提高對野生型病毒(綠色)和Beta變種(橙色)的中和抗體滴度(圖片來源:參考資料[2])
針對受到廣泛關注的Delta變種,接種第三劑疫苗後,中和抗體滴度在18-55歲成人中提高5倍以上,在65-80歲老年人中提高11倍以上(見下圖)。
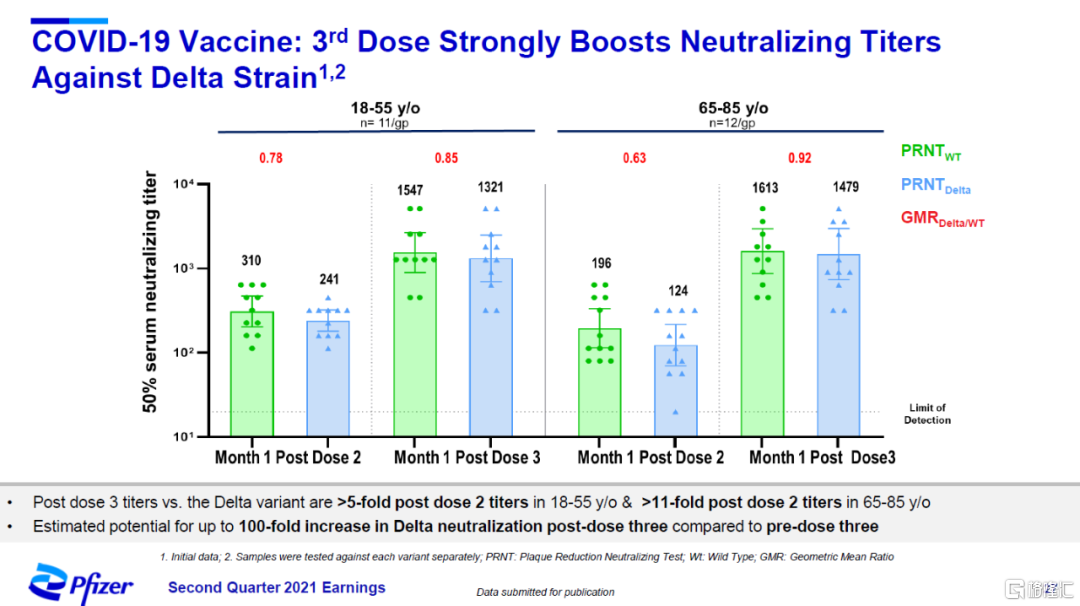
圖片來源:參考資料[2]
該公司正在與監管機構進行討論,預計最早在今年8月遞交關於追加第三劑疫苗接種的緊急使用授權(EUA)申請。同時,針對Delta變種的第一批疫苗已經完成生產,預計臨牀試驗將在8月份開始。
今日,研究人員在預印本網站上公佈了BNT162b2疫苗在3期臨牀試驗中的6個月安全性和效力數據。數據顯示,在接種第二劑疫苗後6個月裏,BNT162b2預防出現症狀的COVID-19的整體效力爲91%。研究人員指出,疫苗的防護效力隨着時間的推移有一定程度的下降,在接種兩劑疫苗之後,防護效力的峯值爲96.2%(接種後7天~2個月),接種後2~4個月,疫苗效力爲90.1%,接種後4~6個月,疫苗效力爲83.7%。
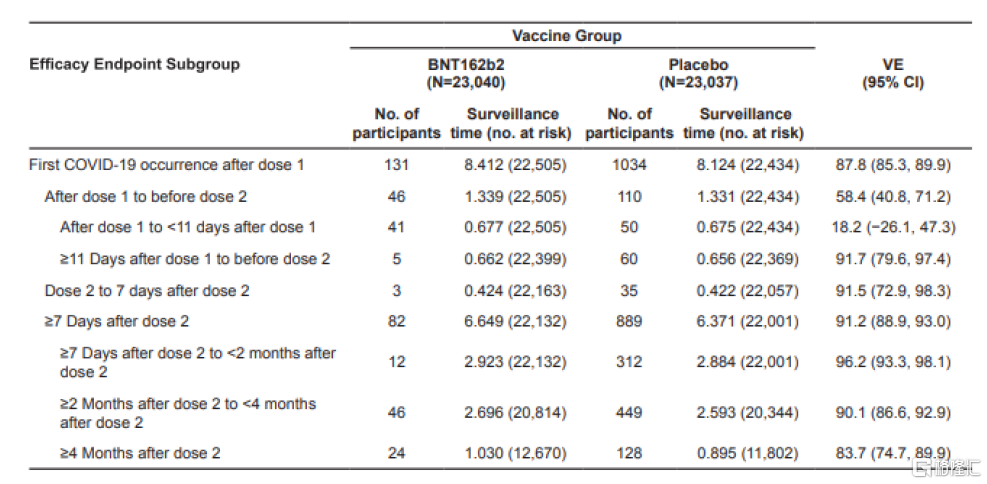
▲接種兩劑疫苗後不同時間段,疫苗的保護效力(圖片來源:參考資料[3])
在預防嚴重COVID-19方面,6個月後總計發現31名患者,其中30名出現在安慰劑組,1名出現在疫苗組,計算出的保護效力爲96.7%。
在文章的討論環節,研究人員指出,在保護出現症狀的COVID-19方面,目前的數據顯示,疫苗效力每兩個月平均下降6%,他們仍然需要繼續對參與者進行隨訪,以進一步理解疫苗保護效力的持久性,以及是否需要增強接種,何時接種的問題。
口服抗病毒療法展現強力活性
由於新冠病毒的不斷突變,以及在全球範圍疫苗接種尚未普及,COVID-19患者仍然需要創新治療方法。
輝瑞公司開發的口服COVID-19療法是一款3CL蛋白酶抑制劑,它在多種冠狀病毒的生命週期中起到重要作用。它的潛在優勢是對目前所有的新冠病毒變種都可以產生作用。
在臨牀前研究中,這一口服3CL蛋白酶抑制劑表現出強力抗病毒活性,在多項檢測中降低病毒載量和改善組織病理學評分。而且,1期臨牀試驗數據顯示它具有良好的安全性和耐受性,在爲期5天的療程中,藥代動力學數據顯示它在體內的水平能夠產生抗病毒效果。
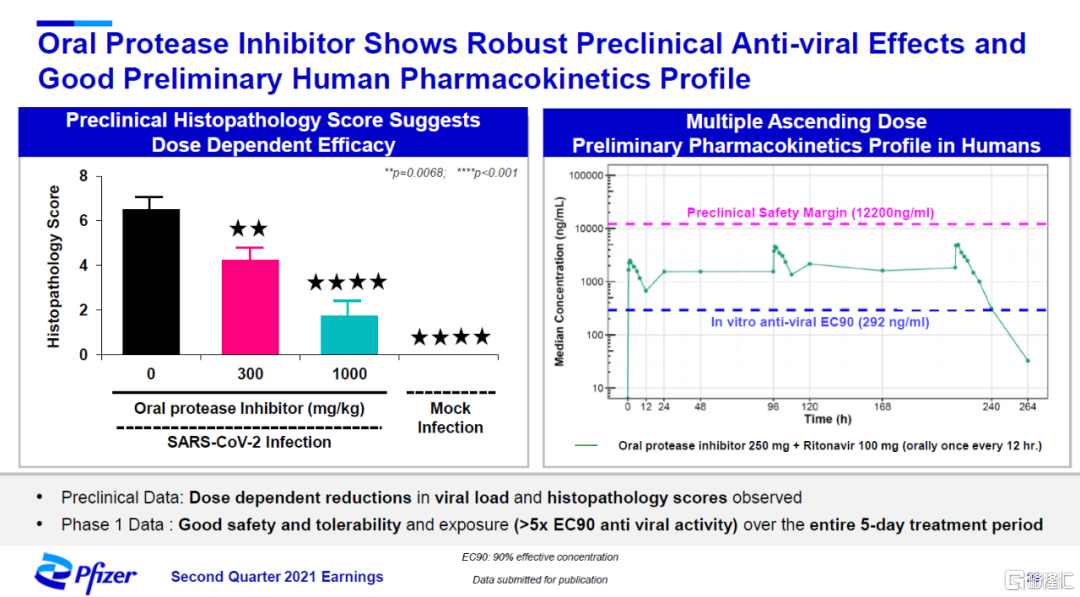
▲輝瑞口服3CL蛋白酶抑制劑的臨牀前和藥代動力學數據(圖片來源:參考資料[2])
輝瑞已經在今年7月啓動2/3期臨牀試驗,預計在第四季度在美國遞交EUA申請。
mRNA流感疫苗即將進入臨牀試驗
mRNA技術平臺正在成爲輝瑞研發的一個重要方向。在新冠疫情爆發以前,輝瑞已經與BioNTech公司達成合作,開發一款高效mRNA流感疫苗。第一代4價mRNA流感疫苗在動物實驗中激發的抗流感病毒抗體水平與已有的包含佐劑的三價蛋白亞基疫苗相當或更高。
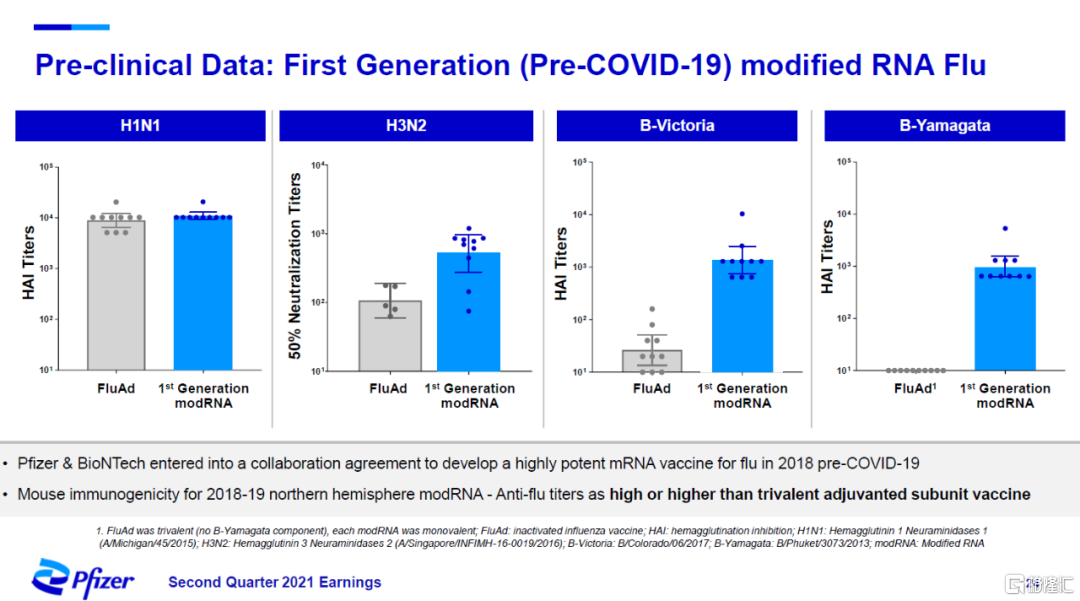
▲第一代mRNA流感疫苗的臨牀前數據(圖片來源:參考資料[2])
新冠疫苗的開發過程加速驗證了mRNA疫苗開發的所有流程,有望大幅度加快mRNA流感疫苗的開發,輝瑞預計mRNA流感疫苗的首個人體試驗將在第三季度展開。
呼吸道合胞病毒(RSV)疫苗展現100%預防效力
RSV是一種全球性疾病,每年在超過5%的老年人和接近10%的高風險成年人中發生。輝瑞開發的RSV疫苗是一款包含融合前穩定RSV F糖蛋白的2價疫苗,它能夠激發針對RSV A和B的高水平中和抗體。在18-55歲成人中進行的2a期病毒挑戰研究中,它在預防出現症狀的RSV疾病方面表現出100%的效力。
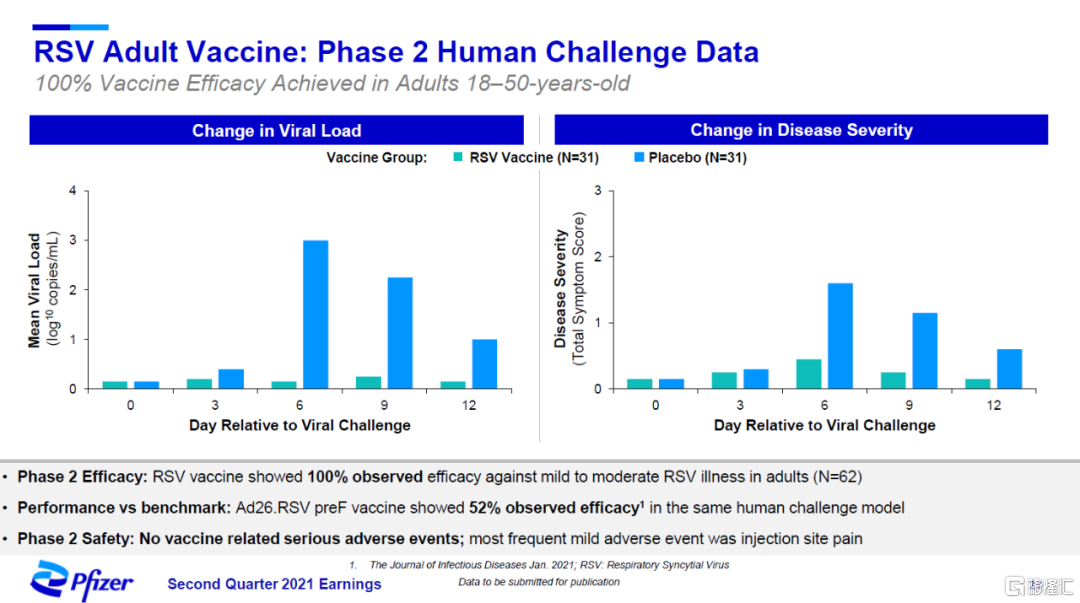
▲RSV成人疫苗在2期病毒挑戰研究中的結果(圖片來源:參考資料[2])
三款基因療法進入3期臨牀試驗
在基因療法方面,輝瑞介紹了分別用於治療血友病A、血友病B和杜氏肌營養不良症(DMD)的基因療法。它們在1/2期臨牀試驗中均表現出良好的療效。治療血友病A的基因療法在一次治療後80周時仍然在患者體內表達具有臨牀意義的凝血因子VIII,在接受治療後頭52周內,患者的年出血率(ABR)爲0。
治療血友病B的基因療法在接受一次治療後第四年時仍然維持穩定的凝血因子IX活性,患者ABR<1。
治療DMD的基因療法在一次治療後2-12個月時表現出穩定的迷你抗肌萎縮蛋白表達水平,以及患者可喜的運動功能改善。
這三款基因療法預計在明年一月(血友病B),或第三季度(血友病A和DMD)獲得3期臨牀試驗結果。
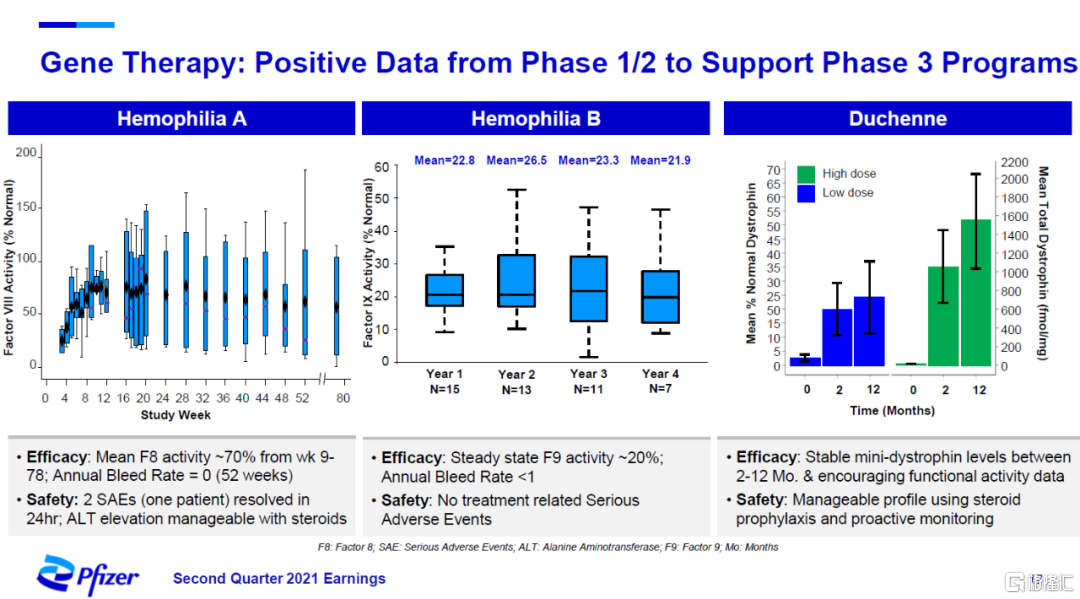
▲治療血友病A(左),血友病B(中),DMD(右)的基因療法的臨牀數據(圖片來源:參考資料[2])
ROBO2配體陷阱顯著降低罕見腎病患者蛋白尿水平
局竈節段性腎小球硬化(FSGS)是一種罕見進行性腎病,大約60%的患者在5-10年內會發展成終末期腎病。
輝瑞公司開發的ROBO2配體陷阱(ligand trap)是一款潛在“first-in-class”,改變疾病進程的創新生物製品,它能夠改善腎臟足細胞的功能,在治療FSGS之外,還可能用於治療其它幾種和足細胞相關的蛋白尿性腎小球疾病。
在2a期臨牀試驗中,中期分析顯示它可以在耐藥性患者中,顯著降低患者尿蛋白肌酐比值(UPCR)。
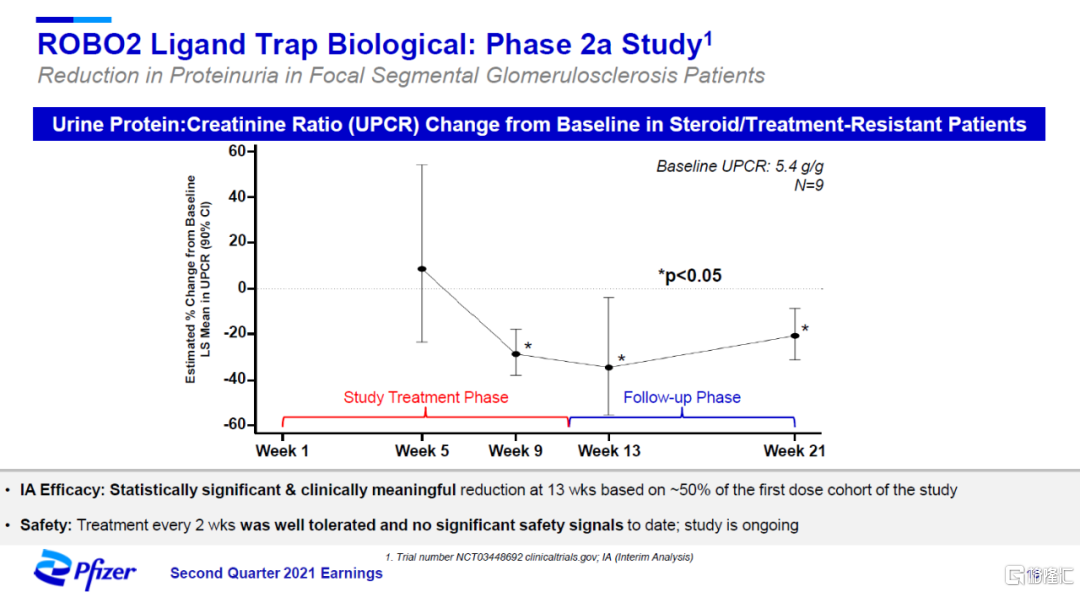
▲ROBO2配體陷阱在2a期臨牀試驗中的表現(圖片來源:參考資料[2])
ARV-471:潛在首款治療乳腺癌的口服PROTAC療法
近日,輝瑞與Arvinas公司達成合作,共同開發和推廣在研靶向雌激素受體(ER)的口服PROTAC蛋白降解劑ARV-471。在Q2電話會議上,輝瑞指出ARV-471已經公佈的1期臨牀試驗結果在接受過多種療法治療的患者中展現出令人信服的療效信號。而且,臨牀前研究顯示,它與CDK4/6抑制劑Ibrance(palbociclib)聯用表現出很好的協同作用。
因此,ARV-471與Ibrance或新一代CDK抑制劑構成的組合療法,有望覆蓋多種雌激素受體(ER)陽性乳腺癌患者。
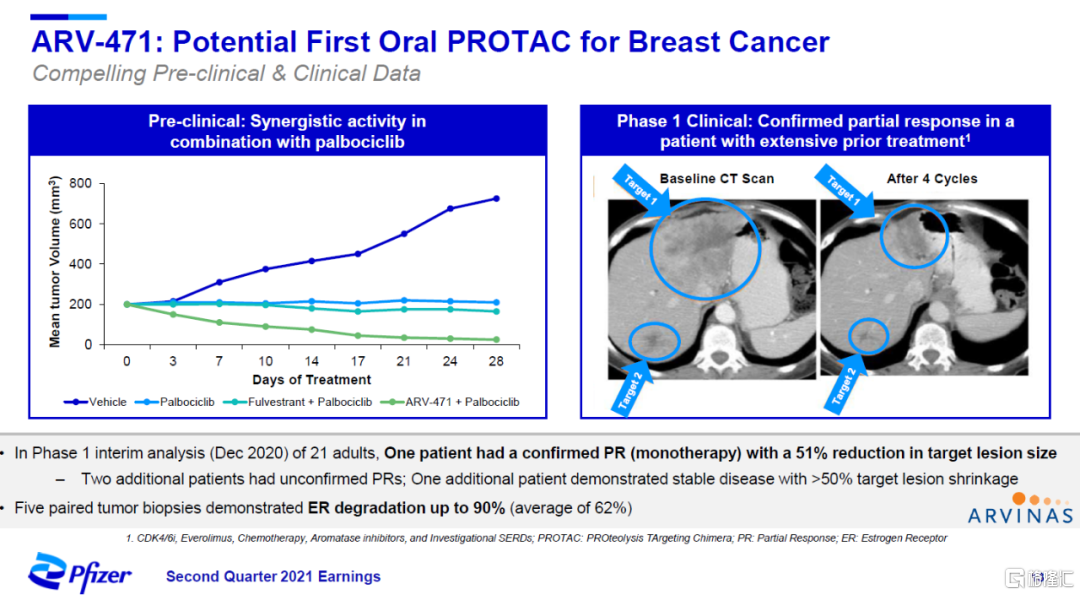
▲ARV-471簡介(圖片來源:參考資料[2])




