格隆匯6月1日|2020年5月31日,復宏漢霖(2696.HK)聯合合作伙伴Accord Healthcare Limited(“Accord”)共同宣佈,歐洲藥品管理局(European Medicines Agency, EMA)人用醫藥產品委員會(Committee for Medicinal Products for Human Use, CHMP)發佈積極審評意見,建議批准HLX02(注射用曲妥珠單抗)用於治療HER2陽性早期乳腺癌、HER2陽性轉移性乳腺癌,以及未經治療的HER2陽性轉移性胃癌或胃/食管交界處腺癌的上市銷售許可申請(Marketing Authorisation Application, MAA)。
根據EMA CHMP的積極審評意見,“HLX02與參照藥赫賽汀(曲妥珠單抗)高度相似,研究數據支持HLX02在質量、安全性與療效等方面與赫賽汀均無顯著差異。”
根據審評流程,CHMP的積極審評意見將被遞交至歐盟委員會(European Commission, EC),EC將參考CHMP的審評意見並在未來2-3個月做出最終決定。若獲得批准,HLX02即可在全部歐盟成員國以及歐洲經濟區國家挪威、冰島和列支敦士登上市銷售,成為進入歐洲市場的第一個“中國籍”單抗生物類似藥,參與生物藥的“世界盃”比賽。根據IQVIA MIDASTM數據估計,2019年原研曲妥珠單抗及其生物類似藥於歐盟及挪威、冰島和列支敦士登的銷售額達到了13.7億美金。
HLX02是由復宏漢霖按照歐盟和中國生物類似藥相關指導自主開發和生產的生物類似藥,其歐盟MAA由復宏漢霖與合作伙伴Accord共同推動,未來HLX02在歐洲的商業化將由Accord負責。目前,HLX02已通過了EMA的GMP現場檢查和GCP檢查,並於2020年4月獲得歐盟GMP認證,表明復宏漢霖已經具備了符合歐盟標準的商業化生產基地和質量管理體系。
在HLX02國際商業化佈局上,復宏漢霖除授予Accord在歐洲、中東、北非地區和部分獨聯體國家共計70餘個國家的HLX02獨家商業化權利之外,公司與Cipla、Mabxience和雅各臣藥業等國際一流的生物製藥企業也達成合作,持續推動HLX02在全球多個國家和地區的商業化進程。
截至目前,復宏漢霖-B(2696.HK)共計涵蓋20多種創新單克隆抗體,並全面推進基於自有抗PD-1單抗HLX10的腫瘤免疫聯合療法。公司已成功上市國內首個生物類似藥漢利康®(利妥昔單抗),2個產品(HLX02曲妥珠單抗、HLX03阿達木單抗)上市申請正在審評中,並獲得優先審評審批資格,有望於今年上市,並同步就10個產品、8個聯合治療方案於全球範圍內開展20多項臨牀試驗,產品對外授權覆蓋全球近100個國家和地區。此外,公司聯合商業合作伙伴Accord推動HLX02向歐洲藥品管理局遞交上市申請,於2020年4月通過歐盟GMP現場核查,有望成為首個在歐盟上市的國產生物類似藥。
據悉,受公司HLX02歐盟上市申請獲推薦批准事件影響,截止發稿時復宏漢霖-B(2696..HK)上漲7.31%至41.85港元。
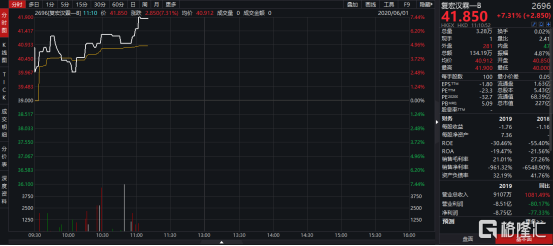
數據來源:WIND,格隆彙整理




